Атомы - это «строительные блоки материи». Все, что имеет массу и занимает пространство (имея объем), состоит из этих крохотных единиц. Это касается воздуха, которым вы дышите, воды, которую вы пьете, и самого вашего тела.
Изотопы являются жизненно важной концепцией в изучении атомов. Химики, физики и геологи используют их, чтобы понять наш мир. Но прежде чем мы сможем объяснить, что такое изотопы или почему они так важны, нам нужно сделать шаг назад и взглянуть на атомы в целом.
Вот это весело
Спорт и наука пересекаются чаще, чем вы думаете. В 2003 году в крупнейшем городе Нью-Мексико появилась новая бейсбольная команда низшей лиги. Как она называется? Изотопы Альбукерке. Отсылка к эпизоду 12-го сезона «Симпсонов», необычное название команды имеет приятный побочный эффект: по необходимости работники примерного стадиона регулярно раздают любопытным фанатам уроки химии.
Наш Атомный Мир
Как вы, наверное, знаете, атомы состоят из трех основных компонентов, два из которых находятся в ядре. Расположенное в центре атомаядропредставляет собой плотно упакованный кластер частиц. Некоторые из этих частиц являютсяпротонами, имеющими положительный электрический заряд.
Доказано, что противоположные заряды притягиваются. Между тем одинаково заряженные тела имеют тенденцию отталкиваться друг от друга. Итак, вот вопрос: как два или более протона с их положительными зарядами могут сосуществовать в одном и том же ядре? Разве они не должны отталкивать друг друга?
Вот тут и появляются нейтроны. Нейтроны - это субатомные частицы, которые имеют общие ядра с протонами. Но нейтроны не обладают электрическим зарядом. Верные своему названию, нейтроны нейтральны, они не заряжены ни положительно, ни отрицательно. Это важный атрибут. В силу своей нейтральности нейтроны могут помешать протонам вытеснить друг друга из ядра.
Элементарно, мой дорогой Ватсон
Вращаются вокруг ядраэлектроны, сверхлегкие частицы с отрицательным зарядом. Электроны облегчают химическую связь, и их движение может производить небольшую вещь, называемую электричеством. Протоны не менее важны. Во-первых, они помогают ученым различать элементы.
Вы могли заметить, что в большинстве версий периодической таблицы каждый квадрат имеет небольшое число, напечатанное в правом верхнем углу над символом элемента. Эта цифра известна какатомный номер. Она сообщает читателю, сколько протонов содержится в атомном ядре определенного элемента. Например, атомный номер кислорода равен восьми. Каждый атом кислорода во Вселенной имеет ядро, содержащее ровно восемь протонов; Не больше, не меньше.
Без этого очень специфического расположения частиц кислород не был бы кислородом. Атомный номер каждого элемента, включая кислород, абсолютно уникален. Никакие два элемента не могут иметь одинаковый атомный номер. Ни у одного другого элемента нет восьми протонов на ядро. Подсчитав количество протонов, можно идентифицировать атом. Точно так же, как атомы кислорода всегда будут иметь восемь протонов, атомы азота всегда будут иметь семь. Это так просто.
Нейтроны не следуют этому примеру. Ядро атома кислорода гарантированно содержит восемь протонов (как мы установили). Однако он также может содержать от четырех до 20 нейтронов. Изотопы - это варианты одного и того же элемента, которые имеют разное количество нейтронов (и, следовательно, потенциально разные физические свойства). Однако они, как правило, обладают одинаковыми химическими свойствами.
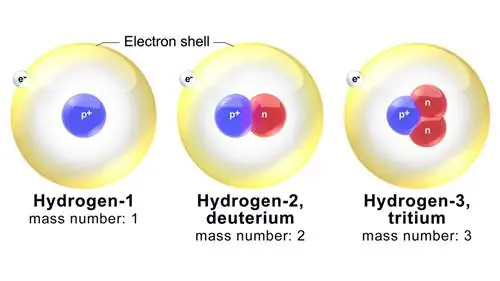
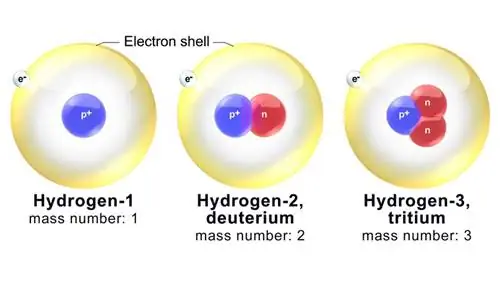
Теперь каждый изотоп назван на основе егомассового числа, которое представляет собой общее количество нейтронов и протонов в атоме. Например, один из наиболее известных изотопов кислорода называется кислород-18 (О-18). У него стандартные восемь протонов плюс 10 нейтронов.
Следовательно, массовое число О-18 равно, как вы уже догадались, 18. У родственного изотопа кислорода-17 (О-17) в ядре на один нейтрон меньше. Таким образом, O-16 имеет одинаковое количество протонов и нейтронов: восемь. Среди этого трио O-16 и O-17 являются более легкими изотопами, а O-16 также является наиболее распространенным изотопом из трех.
Чувство нестабильности
Некоторые комбинации сильнее других. Ученые классифицируют О-16, О-17 и О-18 как стабильные изотопы. В стабильном изотопе силы, создаваемые протонами и нейтронами, удерживают друг друга вместе, навсегда сохраняя ядро неповрежденным.
С другой стороны, ядро радиоактивного изотопа, также называемого «радиоизотопом», нестабильно и со временем распадается.радиоактивный изотоп имеет отношение протонов к нейтронам, которое принципиально неустойчиво в долгосрочной перспективе. Никто не хочет оставаться в этом затруднительном положении. Следовательно, радиоактивные изотопы будут испускать определенные субатомные частицы (и высвобождать энергию), пока не превратятся в хорошие стабильные изотопы.
O-18 стабилен, а кислород-19 (O-19) нет. Последний неизбежно сломается - быстро! В течение 26,88 секунд после создания образец O-19 гарантированно потеряет половину своих атомов в результате радиоактивного распада.
Это означает, что период полураспада О-19 составляет 26,88 секунды. Период полураспада - это время, за которое распадается 50 процентов образца изотопа. Помните эту концепцию; мы собираемся связать его с палеонтологией в следующем разделе.
Но прежде чем мы поговорим об ископаемых, необходимо сделать одно важное замечание. В отличие от кислорода, некоторые элементы вообще не имеют стабильных изотопов. Рассмотрим уран, один из самых известных радиоактивных элементов. В естественном мире существует три изотопа этого тяжелого металла, и все они радиоактивны, а атомные ядра находятся в постоянном состоянии распада. В конце концов, кусок урана превратится в совершенно другой элемент периодической таблицы.
Не пытайтесь смотреть переход в режиме реального времени. Процесс разворачивается очень и очень медленно.
Свидания (и сохранение здоровья)
Уран-238 (U-238), наиболее распространенный изотоп этого элемента, имеет период полураспада около 4,5 миллиардов лет! Постепенно это станет стабильным свинцом-206 (Pb-206). Точно так же уран-235 (U-235) с периодом полураспада 704 миллиона лет превращается в свинец-207 (Pb-207), еще один стабильный изотоп. (И U-238, и U-235 являются примерами встречающихся в природе изотопов.)
Для геологов это очень полезная информация. Скажем, кто-то находит плиту породы, кристаллы циркона которой содержат смесь U-235 и Pb-207. Соотношение этих двух атомов может помочь ученым определить возраст породы.
Вот как: допустим, атомы свинца значительно превосходят по численности своих урановых аналогов. В этом случае вы знаете, что смотрите на довольно старый камень. В конце концов, у урана было достаточно времени, чтобы начать превращаться в свинец. С другой стороны, если верно обратное - и атомы урана более распространены - тогда порода должна быть на более молодой стороне.
Техника, которую мы только что описали, называется радиометрическим датированием. Это акт использования хорошо задокументированных скоростей распада нестабильных изотопов для оценки возраста образцов горных пород и геологических образований. Палеонтологи используют эту стратегию, чтобы определить, сколько времени прошло с момента отложения конкретной окаменелости. (Хотя не всегда возможно датировать образец напрямую.)
Вам не нужно быть любителем предыстории, чтобы ценить изотопы. Практикующие врачи используют некоторые из радиоактивных разновидностей для мониторинга кровотока, изучения роста костей и даже борьбы с раком. Радиоизотопы также использовались, чтобы дать фермерам представление о качестве почвы.
Итак, вот оно. Нечто столь кажущееся абстрактным, как изменчивость нейтронов, влияет на все, от лечения рака до загадок глубокого времени. Наука - это круто.
Часто задаваемые вопросы
Что такое изотопы с примерами?
Изотоп - это атом элемента, который имеет другое число нейтронов, чем другие атомы этого элемента. Примеры изотопов включают водород-1 (протий), углерод-12 (C-12) и углерод-14 (C-14).