Рак считается самой смертельной болезнью во всем мире - в 2004 году он унес жизни 7,4 миллиона человек по всему миру. Он сеет хаос в наших телах, вызывая неконтролируемый рост клеток. Однако благодаря достижениям в лечении рака мы на самом деле движемся в правильном направлении в войне с раком.
На самом деле наши показатели выживаемости улучшаются. С 1975 по 1977 год пятилетняя выживаемость при раке составляла 50 процентов. Перейдем к 1999-2005 гг., и этот показатель вырос до 68 процентов. Это хорошие новости. И по мере того, как мы продолжаем двигаться вперед, надежд становится еще больше. Давайте обсудим несколько многообещающих солдат этой войны.
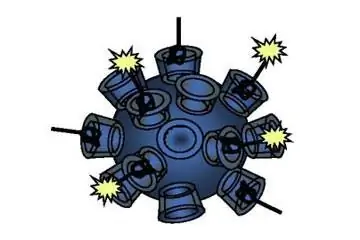
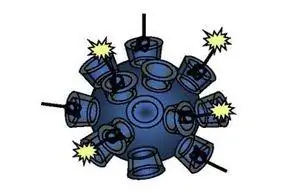
В одной из разработок эти солдаты принимают форму крошечных роботов, называемых наноботами, которые проникают в наши клетки, чтобы исправить генетические мутации, вызывающие рак. Исследователи из Калифорнийского технологического института (Калифорнийский технологический институт) взяли концепцию наноботов и объединили ее с технологией, разработанной более десяти лет назад, под названиемРНК-интерференция При РНК-интерференции частицы проникают в клетку и мешают генетический код. В этом случае он идет за частью, содержащей мутацию. Калифорнийская команда обнаружила, что они могут поместить эти частицы внутрь нанороботов, отправить их в кровоток и начать уничтожать раковые мутации. Эта тактика в настоящее время тестируется на 15 пациентах в ходе I фазы клинических испытаний, спонсируемых Caldano Pharmaceuticals.
Но наноботы - это только начало того, что происходит в области исследований рака.
Больше самых многообещающих методов лечения рака
Другой областью лечения, набирающей популярность, являетсятаргетная терапия рака В рамках этого подхода разрабатываются лекарства, которые останавливают сверхактивное производство клеток, присущее раку. Результаты достигаются по-разному в зависимости от типа рака. Например, таргетную терапию можно использовать для уничтожения клеток, привлечения иммунной системы к атаке раковых клеток или блокирования ферментов, вызывающих гиперактивный рост. В настоящее время несколько таргетных методов лечения были одобрены FDA для использования на людях, в то время как другие все еще находятся на стадии исследований.
В таргетной терапии мы упоминали об использовании собственной иммунной системы для борьбы с раком. Как вы, наверное, знаете, наша иммунная система помогает защитить нас от болезней. Для борьбы с раком необходимо, чтобы иммунная система распознала, что раковые клетки функционируют ненормально. Вот тут-то и появляется другое обнадеживающее лечение -иммунотерапия. Исследователи обнаружили, что наша иммунная система может бороться с раком, особенно с раком крови. Существует три метода иммунотерапии:
- Вакцины: этот метод вызывает реакцию в организме, которая заставляет иммунную систему атаковать раковые клетки.
- Клеточное лечение: при этом типе иммунотерапии пациенты получают донорские лейкоциты, которые распознают раковые клетки как атипичные и поэтому уничтожают их.
- Антитела: этот процесс включает антиген, вызывающий выработку антител, которые помечают раковые клетки как «плохие», что служит сигналом для атаки иммунной системы.
[источник: Общество лейкемии и лимфомы]
Если мы каким-то образом создадим среду, в которой раковые клетки больше не смогут развиваться, есть надежда, что они перестанут расти и умрут. Это идея использованияантиангиогенеза для лечения рака. Ангиогенез - это рост новых кровеносных сосудов, которые сохраняют ткани нашего тела красивыми и здоровыми. Нашим клеткам нужна здоровая ткань, чтобы жить и расти, но раковым клеткам здоровая ткань нужна даже больше, чем нормальным клеткам. Отключите ангиогенез, испортив белки, отвечающие за этот процесс, и вы просто лишите раковые клетки способности продолжать расти. Однако использование белков для остановки ангиогенеза не является особенно новым. На самом деле, некоторые методы лечения уже проходят клинические испытания, и FDA только что одобрило лекарство, которое воздействует на клетки слизистой оболочки кровеносных сосудов для борьбы с метастатическим раком.
Чтобы узнать, что нового в ангиогенезе и лечении рака, продолжайте читать.
Еще больше оружия в войне с раком
Мы только что упомянули, что использование белков для остановки ангиогенеза не является чем-то новым в лечении рака. Что нового, так это идея, появившаяся в результате сотрудничества Кристин Ван Влит из Массачусетского технологического института и Айры Херман из Медицинской школы Университета Тафтса. Эти двое изучают связь междуперицитами и нашим здоровьем. Перциты - это клетки, которые окружают наши кровеносные сосуды и сокращаются. Van Vliet и Herman показали, что это сокращение может запускать ангиогенез. Если это так, контроль сокращения может стимулировать или ингибировать ангиогенез.
До сих пор мы обсуждали методы лечения, которые кажутся взвешенными и стратегическими. Но что, если бы мы могли просто войти, взорвать рак и покончить с этим? Хотя только в лабораторных культурах, Национальный институт стандартов и технологий сделал именно это. Исследователи применили двухсторонний подход к технике бомбы и объединили антитело снанотрубкой По сути, нанотрубка взрывает опухолевые клетки, в то время как антитело начинает работать, искажая белок. который работает на стороне опухолей. Время покажет, смогут ли эти два воина выйти в бой за пределы клеточной культуры и работать на мышах.
Взрыв рака и каждое новое открытие в этой борьбе помогает. По мере продвижения вперед мы можем надеяться на окончательное отступление рака. Тем не менее, пожалуй, лучшей тактикой, чем любое новое лечение, по-прежнему являются профилактика и ранняя диагностика, последние достижения, которые мы обсудим здесь. Профилактика и ранняя диагностика являются ключом к выживанию. Мы уже знакомы с такими стратегиями, как маммография и колоноскопия, но что, если бы мы могли начать обнаружение еще раньше? Мы можем. Фактически, команда детской больницы Mattel UCLA используетнанодиагностику для проверки новорожденных на возможность развития определенных заболеваний в более позднем возрасте, включая рак. Они делают это, беря образец ткани или крови у новорожденного, а затем берут наноразмерные фрагменты ДНК ребенка и пропускают их через 900 000 генетических последовательностей, уже связанных с заболеваниями, чтобы увидеть, есть ли совпадение. Есть совпадение? Тогда у вас есть веская причина принять определенные превентивные меры в жизни этого ребенка.